Ciencia
El mundo científico contiene un gran cúmulo de conocimientos que permite a la humanidad a vivir de la manera en que lo hace. Explore la base de documentos y trabajos sobre las ciencias naturales y formales.
Documentos 259.651 - 259.725 de 497.510
-
![Itegración por sustitución]()
Itegración por sustitución
Alan Caballero VillavicencioINTEGACION POR SUSTITUCIÓN o CAMBIO DE VARIABLE Pasos para integrar por método de sustitución para la integral: Donde m= Se hace cambio de variable Derivar con respecto a Despejar Sustituir los términos encontrados en la integral Tenemos que , y que entonces se sustituyen en Por lo tanto tenemos que:
-
Itegradora IMC Etapa 3
chuychapaActividad Integradora Elaboración de un cuadro QQQ. (Qué veo, qué no veo y qué infiero) La estrategia QQQ permite descubrir las relaciones de las partes de un todo (entorno o tema) a partir de un razonamiento crítico, creativo e hipotético. Sus características son: - Qué veo: es todo aquello que
-
Itegrales
asdfghjkl1996Introducción El Cálculo se inventó en el siglo XVII como un medio para estudiar los problemas en que intervenía el movimiento. EI algebra y la trigonometría pueden servir para estudiar los objetos que se mueven con velocidad constante ante a lo largo de una trayectoria rectilínea o circular, pero si
-
![ÍTEM I EL AGUA Y SUS CARACTERÍSTICAS]()
ÍTEM I EL AGUA Y SUS CARACTERÍSTICAS
nanimecheEscuela Lo Arcaya Pirque Asignatura: Ciencias Naturales Prueba de Unidad Profesora: Nancy Díaz C. Curso: 2º Básico Nombre: _ Fecha: _ Nota: _ OBJETIVOS DE APRENDIZAJES ITEM PUNTAJE Ideal Real OA9 Observar y describir, por medio de la investigación experimental , algunas características del agua… I 24 OA10 Identificar y
-
ITEM SELECCIÓN ÚNICA.
dipropous- ITEM SELECCIÓN ÚNICA. (1 puntos cada una) Total: 20.Lee muy bien cada una de las siguientes aseveraciones y luego encierra en un círculo la alternativa correcta, recuerdaque no pueden haber borrones o marcar dos alternativas, porque será considerado incorrecto.1. La historia se desarrolla en:a) Una ciudad muy habitadab) Una
-
![ITEMS DEL PROYECTO DE INVESTIGACION]()
ITEMS DEL PROYECTO DE INVESTIGACION
Sylvana FloresTRABAJO ENCARGADO TEMA : ITEMS DEL PROYECTO DE INVESTIGACION Responder a las preguntas que permitirán formular un proyecto de investigación. 1. ¿Qué? El problema Implementación de una plataforma virtual como estrategia para la mejora de los aprendizajes del área de EPT en los alumnos del tercero de secundaria de la
-
![Items más importantes de los capítulos del Nivel Químico, Citología e Histología]()
Items más importantes de los capítulos del Nivel Químico, Citología e Histología
Ricardo CoverumiPROLOGO Este libro de bolsillo se ha escrito con el objetivo principal, de presentar, los ítems más importantes de los capítulos del Nivel Químico, Citología e Histología, en función a los últimos 10 años de exámenes de Admisión en la Universidad de Tumbes. Las preguntas están ordenadas gradualmente, desarrollándose en
-
Iter Criminis
diego30Argumento analógico es definido como un instrumento al servicio del principio de conservación de las normas, cuyos elementos son: la existencia de una norma que se tiene como referencia, la existencia de una laguna legal y la ratio legis. La analogía justifica trasladar la solución legalmente prevista para un caso
-
Iter Criminis
gypsy88DEBE LIMITARSE LA LIBERTAD DE INFORMACIÓN EN LOS MEDIO DE COMUNICACIÓN DEL INTERÉS PÚBLICO? Actualmente la libertad de información está en su mayor apogeo gracias a la tecnología como la televisión, la Radio e Internet, que sirven como un medio de información ya que es un derecho del pueblo que
-
Iter Criminis
tacquiIterCriminis. Con este nombre se conoce el conjunto de acontecimientos que va desde que el sujeto idea un delito hasta su consumación y/o agotamiento. También recibe las denominaciones de: a) “grados de desarrollo del delito”, b) “etapas de perfeccionamiento del delito”. En nuestro país está consagrado en los Arts. 7
-
Iter Criminis
bamn881001ITER CRIMINIS El delito es un fenómeno psíquico-físico, ya que puede surgir en la mente del autor, se exterioriza a través de la ejecución de una acción que puede producir un resultado. Este camino que sigue el delito se llama iter criminis, que va desde la idea delictiva hasta la
-
![ITERACIÓN SIMPLE DE PUNTO FIJO (METODO ABIERTO)]()
ITERACIÓN SIMPLE DE PUNTO FIJO (METODO ABIERTO)
Mario VargasIteración Simple de Punto Fijo ITERACIÓN SIMPLE DE PUNTO FIJO (METODO ABIERTO) Métodos Abiertos: Hay un segundo tipo de métodos que aprovechan raíces de ecuaciones, que son los llamados “métodos abiertos”. Estos métodos tienen características importantes de recalcar, como por ejemplo: sólo requieren un valor inicial o un par, pero
-
Iteracion y convergencia de sistemas de ecuaciones
safetyIteracion y convergencia de sistemas de ecuaciones Conceptos básicos En general, en todos los procesos iterativos para resolver el sistema Ax=b se recurre a una cierta matriz Q, llamada matriz descomposición, escogida de tal forma que el problema original adopte la forma equivalente: Qx = (Q-A)x+b (62) La ecuación (62)
-
![ITF, IMPUESTO A LAS TRANSACCIONES FINANCIERAS]()
ITF, IMPUESTO A LAS TRANSACCIONES FINANCIERAS
CELSOLAS ITF (IMPUESTO A LAS TRANSACCIONES FINANCIERAS) El Impuesto a las Transacciones Financieras (ITF), impuesto que grava básicamente todos los retiros o depósitos en cualquier modalidad de cuenta abierta en alguna de las empresas del sistema financiero nacional, así como la adquisición de cheques de gerencia, giros, certificados bancarios u
-
ITIL GESTION DE SERVICIOS
andhers79La fase de Estrategia del Servicio es central al concepto de Ciclo de vida del servicio y tiene como principal objetivo convertir la Gestión del Servicio en un activo estratégico. Para conseguir este objetivo es imprescindible determinar en primera instancia qué servicios deben ser prestados y por qué han de
-
![Itinerario de viaje.]()
Itinerario de viaje.
pminjares2015Itinerario de viaje. Integrantes: 1. Juan Pablo Corrales 2. José Alán Velarde 3. Damaris Elsa Reyes 4. Bryan A. Minjares Continente a visitar: CONTINENTE AMERICANO Fecha del viaje: 02 DE OCTUBRE DE 2015 ¿Qué llevarán en la maleta? Pasajero1: * Documentos de viaje: Identificación Oficial (Pasaporte y Visa), * Dinero
-
![Itinerario Presidente Peru]()
Itinerario Presidente Peru
Kevin RMITINERARIO DEL PRESIDENTE Y MISA DEL TE DEUM La mañana del 28 de julio, el Arzobispo de Lima celebra la Misa y Te Deum, himno de agradecimiento a Dios, como manda la Iglesia Católica. A la misa acuden las personalidades más importantes junto con el Presidente de la República. La
-
![Itinerarios]()
Itinerarios
Luly013FUNDAMENTACIÓN "Saber no es suficiente, debemos aplicar. Desear no es suficiente, debemos hacer". Johann W. Von Goethe. La matemática es el arte de calcular para resolver problemas de una manera sencilla y poder aplicar sus soluciones en nuestra vida cotidiana, pero no solo se trata de fórmulas engorrosas sino también
-
![ITR USOS ADECUADOS DE METODOS ANTICONCEPTIVOS PASTILLA ANTICONCEPTIVA]()
ITR USOS ADECUADOS DE METODOS ANTICONCEPTIVOS PASTILLA ANTICONCEPTIVA
Eliz LomeliITR USOS ADECUADOS DE METODOS ANTICONCEPTIVOS PASTILLA ANTICONCEPTIVA INSTITUTO TECNOLOGICO ROOSEVELT PROYECTO INTEGRADOR USOS ADECUADOS DE MÉTODOS ANTICONCEPTIVOS (PASTILLA ANTICONCEPTIVA) CUELLAR MARTINEZ MARISOL LOMELI RAMIREZ CINTIA ELIZABETH 17/05/2021 CONTEXTO El nacimiento de la píldora anticonceptiva se remota hace más de 50 años atrás, siendo uno de los acontecimientos en la
-
Itroduccion A La Ingenieria
aepincayCapítulo 1 El problema: Tabaquismo en la UUEES Enunciado del problema Como estudiantes universitarios hemos visto una cantidad considerable de estudiantes adolecentes teniendo este habito del tabaquismo adolecente de 17-24 años que fuman de 1-3 cigarrillos aproximadamente al día. En esta investigación pretendemos analizar y responder las inquietudes del porque
-
Itroduccion De La Filosofia
hm3dsignsIntroduccion a la Filosofia 1- ENUMERE Y EXPLIQUE LAS CRÍTICAS QUE EVANDRO AGAZZI ET AL. HACEN CONTRA LA IDEA DE QUE EL MÉTODO CIENCTIFICO SE BASA EN LA INDUCCIÓN. COMPÁRELA CON LAS DE Chalmers, Y CON LAS QUE SE HAN HECHO EN CLASES 1- Las críticas que hace Afazzi son
-
Itroduction
jredIntroduction Many professional footballers are unknowingly teachers of nonlinear differential equations. That can be seen in the quality and curvature that many of them apply to make their free throws, that having been executed correctly wonders become a goal, for example; just remember that free kick from David Beckham England
-
![ITS (Infecciones de transmisión Sexual)]()
ITS (Infecciones de transmisión Sexual)
luisfelipefdzmITS (Infecciones de transmisión Sexual) Las infecciones de transmisión sexual o ITS Son Aquellas que pueden transmitirse de una persona a otra durante una relación sexual ya sea vaginal , oral o anal… LA INFECCION SE PUEDE ADQUIRIR CON EL CONTACTO DIRECTO AUNQUE NO HAYA PENETRACION, o sea no solo
-
ITS (unas Cuantas)
Índice Portada…1 Índice.2 Introducción.3 Treponema pállidum (Sifilis).4-5 Gonorrea (Neisseria gonorrhoeae).6-7 Herpes genital (HSV-2).8-9 Conclusión.10 Comentario…11 Bibliografia y Linkografia.12 Introducción Son un grupo de enfermedades que se contagian durante las relaciones sexuales sin protección. Son causadas por virus, bacterias, hongos y otros gérmenes microscópicos. Atacan a personas de cualquier edad y
-
![ITS Gonorrea]()
ITS Gonorrea
KarlaD17Gonorrea I) Recomendación La gonorrea es una enfermedad venérea que afecta a toda la población incluso a los recién nacido (lógicamente los recién nacidos se infectan por medio del parto), niños y adolescentes. Normalmente el grupo que más sufre de estas infecciones son los adolescentes, por falta de información, por
-
ITS Infecciones De Transición Sexual
mony1995¿Sabes que son las ITS y el VIH? Generalidades Información de Infecciones de Transmisión Sexual Las infecciones de transmisión sexual (ITS) son un problema de salud frecuente con consecuencias potencialmente graves, que incluyen infertilidad, enfermedad crónica y muerte. Asimismo, las ITS aumentan la transmisión de la infección por el VIH.
-
Its Kind Of A Funny Story
angtc131. Para iniciar con tu estudio y análisis del mercado, describe detalladamente cada uno de los elementos de la mezcla de mercadotecnia y su importancia en el proceso: 1. Producto: Coca-cola: 2. Promoción 3. Precio 4. Plaza 5. Personal 6. Proceso 7. Presentación 2. Diseña la imagen de la envoltura
-
ITS o infecciones de transmisión sexual
70255342INTRODUCCION El presente ensayo dará a conocer un poco sobre lo que he investigado sobre las “ITS” o mejor dicho las Infecciones de Transmisión Sexual, les diré el por qué elegí este tema, para empezar me llamo un poco la atención de primero pero conforme fui investigando me gusto aun
-
![ITS, INFECCIONES DE TRANSMISIÓN SEXUAL]()
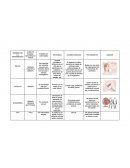
ITS, INFECCIONES DE TRANSMISIÓN SEXUAL
Camila_Perez.5NOMBRE DE LA ENFERMEDAD AGENTE CAUSAL: BACTERIA O VIRUS FORMA DE CONTAGIO SINTOMAS CONSECUENCIAS TRATAMIENTO IMAGEN SIFILIS Bacteria treponema pallidum. Se transmite por contacto sexual o por contacto directo con la boca o heridas contagiadas. Ulceras genitales o chancros en el sitio por el penetraron las bacterias, lesiones en la
-
![ITSAV verde “un proyecto de vida”]()
ITSAV verde “un proyecto de vida”
Guadalupe167ITSAV verde “un proyecto de vida” DESARROLLADOR DEL PROYECTO: Ing. Jeremías Roque Tolentino REPORTE DE PROYECTO Nombre del alumno(a): GUADALUPE CASTRO DECEANO No. de Control: 206Z0250 Semestre y grupo: 5 SEMESTRE Carrera: INGENIERIA INDUSTRIAL (SABATINO) Fotos Nombre científico Citrus limón Nombre vulgar Árbol de limón Origen Sureste asiático y malasia
-
Itsmo De Panama
Daniel14flEl istmo de Panamá es un accidente geográfico localizado en Panamá, entre los océanos Pacífico y el Atlántico, que une a América del Sur y a América Central. Tiene una longitud de unos 700 kilómetros, su anchura varía entre cincuenta y doscientos kilómetros, y está accidentado por la cordillera de
-
ITU EN PEDIATRIA
ysa1INTRODUCCION El término genérico de infección urinaria implica el hallazgo en orina de microorganismos, habitualmente bacterias, en título elevado, más de 100.000 unidades formadoras de colonias (CFU) por ml. Sin embargo esta definición clásica de bacteriuria significativa no es excluyente, porque existen determinadas situaciones en las que recuentos inferiores son
-
![ITU OPINION]()
ITU OPINION
Diana CastilloReflexiones: ¿Cuáles son las 3 cosas que has aprendido de este caso? Responder de manera individual los integrantes del equipo. Reflexione sobre su aprendizaje sobre el caso desarrollado * La técnica de recolección de muestra en orina, en una ITU baja o alta el diagnóstico clínico tiene que apoyarse en
-
![Ítulo. Tiro Parabólico (Composición de dos movimientos)]()
Ítulo. Tiro Parabólico (Composición de dos movimientos)
CarolinaBerUNAM FACULTAD DE CIENCIAS Laboratorio de Mecánica Título. Tiro Parabólico (Composición de dos movimientos) Abstract Usando Tracker y un sistema en el cuál se dispara una pelota a un ángulo fijo de 45 grados se comprobaron las características de un tiro parabólico ideal (sin fuerzas externas más que la gravitacional
-
Itv Negocios
arman2207comunicadas de un modo preciso mediante la expresión vocal, pero hay algunasmás fáciles de reconocer como la alegría y el odioEn general, podemos afirmar entonces que nuestras percepciones de señalesvocales se combinan con otros estímulos verbales o no verbales creándose unabase de comunicación.En cuanto al desarrollo de las habilidades no
-
Itzel File
itzelD“LA EDUCACIÓN” Mi nombre es Diana Itzel Cervantes León durante mis 11 años he estudiado en diferentes instituciones de las cuales recuerdo a la Hispano, La Raza, Colegio América Latina, Zamá y en la actualidad estoy por terminar mis estudios de preparatoria en UVM campus Hispano. Me he estado preparando
-
It’s Compliated es una comedia romántica
danieltiger“It’s Compliated” “It’s Complicated” es una comedia romántica que representa a una pareja divorciada (Meryl Streep y Alec Baldwin) que se vuelven a reencontrar por una noche, ahí es donde comienzan a vivir una aventura, complicando la vida de ambos. Esta abarca principalmente el tema de las relaciones matrimoniales en
-
![Iujiok]()
Iujiok
elianagarcia89EVALUACION ACADEMICA Alumno: Ruv: No.Documento: Grado Periodo Año Escolar Director Grupo: DIMENSION COGNITIVA Establece relaciones espaciales de su entorno y en actividades escritas como: arriba, adelante, atrás,Izquierda, derecha,adentro y afuera. Escribe, identifica, cuantifica, enuncia del uno a un numero indicado_ Comprende ordenando y armardo una historia corta en secuencia. Muestra
-
IUPAC
katherineC18AGUA DESTILADA: Es aquella que como todo tipo de agua está compuesta por dos átomos de hidrógeno y uno de oxígeno, cuya molécula se representa químicamente por la fórmula H2O y que mediante el proceso de destilación se le han eliminado las impurezas e iones. La destilación es un método
-
IUPAC
HAuditore420podrá hacer esto? Además la paraestatal se debe comprometer a limpiar las zonas dañadas, sin dejar el trabajo a terceros. En ciertos casos Protección Civil puede apoyar con bomberos, para el control de incendios y exposiciones. Sin embargo ¿qué pasa cuando la fauna local se ve afectada, ¿quién se encarga
-
![IUPAC, SISTEMA STOCK E TRADICIONAL, OXIDOS, ANHIDRIDOS E HIDROXIDOS]()
IUPAC, SISTEMA STOCK E TRADICIONAL, OXIDOS, ANHIDRIDOS E HIDROXIDOS
unhombremenos1) Defina IUPAC, nomenclatura, oxido básico, óxidos ácidos u anhídridos, bases o hidróxidos: IUPAC: La Unión Internacional de Química Pura y Aplicada, más conocida por sus siglas en inglés IUPAC, es un grupo de trabajo que tiene como miembros a las sociedades nacionales de química. Es la autoridad reconocida en
-
Ius Cogens
dianathomaEL DERECHO INTERNACIONAL IMPONE LIMITES A LA SOBERANÍA COLOMBIANA? Pues bien, ante el interrogante damos un vistazo a la Soberanía en nuestro ordenamiento jurídico Colombiano1, observando además cómo los tratadistas2 se han ocupado de estudiar que ésta se asume como la potestad del pueblo en decidir su forma de gobierno,
-
Ius Drecho
axenegTesis Semanario Judicial de la Federación Octava Época 228 583 1 de 1 TERCER TRIBUNAL COLEGIADO EN MATERIA ADMINISTRATIVA DEL PRIMER CIRCUITO. III, Segunda Parte-1, Enero a Junio de 1989 Pág. 419 Tesis Aislada(Administrativa) [TA]; 8a. Época; T.C.C.; S.J.F.; III, Segunda Parte-1, Enero a Junio de 1989; Pág. 419 INTERPRETACION
-
IUS FAS
AuAntonietaGNuestra voz Derecho corresponde a la voz latina Ius, que comprende la noción del Derecho, Celso, lo definió como el arte de lo bueno y lo justo, es decir, aquello que en la conciencia social se consideraba como justo y bueno. Por otro lado, el Fas, expresaba la voluntad de
-
IUS PUNENDI
caceresv85QUE ES EL IUS PUNIENDI De manera histórica el Derecho Penal ha sido visto como un poder restrictivo, represivo, es por ello que hoy en día existe un amplio consenso en delimitar los fines punitivos del Estado a través de la Constitución, ya que este Poder se realiza mediante normas
-
IUS PUNIENDI
lourdeslamedaIUS PUNIENDI Índice 1 Introducción: Derecho Penal objetivo y Derecho Penal subjetivo 2 Fundamento del ius puniendi estatal 3 Naturaleza del ius puniendi 4 Titular del ius puniendi 5 Límites del ius puniendi: límites "formales" y límite "materiales" 5.1 Límite Formales 5.2 Límites Materiales 6 Referencias Ius puniendi es una
-
![IUS según a Mario Bunge]()
IUS según a Mario Bunge
Karen LozanoiINTRODUCCION AL ESTUDIO DEL DERECHO En muchas ocasiones pensamos que el derecho (IUS) no está nada relacionado con la ciencia, la filosofía, el arte o algún método científico, sin embargo, estamos muy equivocados, al derecho se le dan distintos sentidos: 1) Derecho como facultad o derecho subjetivo; 2) Derecho como
-
Iusmarxismo
xxangelxxIus marxismo Ius marxismo En el siglo XIX apareció por primera vez el marxismo, corriente de pensamiento y acción que define la época contemporánea. Para Marx, las tesis en el campo del derecho se refieren a éste como una superestructura que se deriva de la estructura económica sobre la que
-
Iusmarxismo En México
bigtaveraPartiendo del punto de vista que el iusmarxismo es un mero reflejo de condiciones e instrumento de conveniencias económicas, que el Derecho no puede separarse nunca de la configuración económica y desarrollo cultural de la sociedad que lo condiciona, además de que es un conjunto de relaciones sociales, en especial
-
Iusnaturalismo
luisa9706El iusnaturalismo (del latín ius, "derecho", y natura, "naturaleza") es una corriente de la filosofía del Derecho que afirma que al menos una parte de las normas convencionales del Derecho y la moral están asentadas en principios universales e inmutables; este conjunto de normas conforman el derecho natural. El origen
-
IUSNATURALISMO
ibethjoselinachaFundamentos de la concepción del derecho Iusnaturalista. Para la concepción iusnaturalista el fundamento de la experiencia jurídica está en la justicia, y el derecho natural es el que establece lo justo de modo universalmente válido. Lo explican a partir del orden divino o del orden de la naturaleza. Así, en
-
![IUSNATURALISMO PROSIGUE]()
IUSNATURALISMO PROSIGUE
valeriacqdIUSNATURALISMO PROSIGUE NOCIONES PREELIMINARES DEL IUSNATURALISMO: el iusnaturalismo es la corriente de pensamiento que tienen como eje fundamental el Derecho Natural, entendido como el conjunto de normas o preceptos que nacen de la misma naturaleza humana, pero desde el punto de vista filosófico, el termino naturaleza, tiene muchas acepciones, o
-
IUSNATURALISMO VS. IUSPOSITIVISMO
tatavelazcoTRABAJO INTRODUCCION A LA FILOSOFIA TEMA: IUSNATURALISMO VS. IUSPOSITIVISMO OBJETO DEL DERECHO ¿El derecho es un arte, una ciencia, una técnica o puede pensarse que de las anteriores tiene un poco? El Derecho se encuentra directamente relacionado con cada uno de los anteriores conceptos, no se podría encasillar al Derecho
-
![IUSNATURLISMO VS. POSITIVISMO]()
IUSNATURLISMO VS. POSITIVISMO
illanDerecho natural El iusnaturalismo o Derecho natural es un enfoque filosófico del derecho que postula la existencia de derechos del hombre universales, anteriores y superiores (o independientes) al ordenamiento jurídico positivo, fundados en la naturaleza humana. El derecho natural esta en el corazon del hombre. Contenido [ocultar] • 1 Introducción
-
Iuspositivismo Desde Su Concepción Formalista – Jurídica
merishkasmIUSPOSITIVISMO DESDE SU CONCEPCIÓN FORMALISTA – JURÍDICA. CAPÍTULO 1. IUPOSITIVISMO (POSITIVISMO). 1.1. GENERALIDADES. El iuspositivismo, también conocido como positivismo jurídico, es una corriente de pensamiento jurídico. La principal tesis del iuspositivismo es la separación entre moral y Derecho, que supone un rechazo a toda relación conceptual vinculante entre ambos. El
-
IV PRÁCTICA DE UNIDAD ESTADISTICA APLICADA A LA ADMINISTRACION I.
aries18UNIVERSIDAD NACIONAL DE TUMBES UNT FACULTAD DE CIENCIAS ECONOMICAS ESCUELA ACADEMICO PROFESIONAL DE ADMINISTRACIÓN UNT http:/definanzas.com/wp-content/uploads/economia.jpg http:/www.muyinternet.com/wp-content/uploads/2010/06/economia-digital.jpg http:/quisqueyainternacional.net/blog/wp-content/uploads/2007/11/economia.jpg IV PRÁCTICA DE UNIDAD ESTADISTICA APLICADA A LA ADMINISTRACION I. 1. Una máquina expendedora de refrescos, se diseñó para despachar, en promedio, 7 onzas de bebida por vaso. En una prueba de
-
![IV SECUENCIA DIDACTICA]()
IV SECUENCIA DIDACTICA
Iram OrdoñezIV SECUENCIA DIDACTICA 4.1 Objetivos Los propósitos: Reconocer e identificar la importancia y trascendencia de la comunicación, así como reconocer los diferentes tipos de lenguaje, las variaciones y las cualidades de la Comunicación. Problema Real del Entorno: Crear un entorno positivo y valorativo en los estudiantes en su forma de
-
![IV SEMESTRE,SECCION1 INVESTIGACION SOCIAL CUALITATIVA]()
IV SEMESTRE,SECCION1 INVESTIGACION SOCIAL CUALITATIVA
marylocaREPÚBLICA BOLIVARIANA DE VENEZUELA MINISTERIO DEL PODER POPULAR PARA LA DEFENSA UNIVERSIDAD NACIONAL EXPERIMENTAL POLITÉCNICA DE LA FUERZA ARMADA BOLIVARIANA UNEFA-NUCLEO VARGAS IV SEMESTRE,SECCION1 INVESTIGACION SOCIAL CUALITATIVA Profesor: Carlos Hernandez Estudiantes: Valero Maryc C.I:17.153.848 Castro Franci C.I: 18.323.324 Barrios Florangel C.I: 22.280.728 Cardona Visaydy C.I:20.559.607 Salazar Loengry C.I: 21.192.702 Tovar
-
Iva
pandirrisEl 'IVA' es un impuesto indirecto sobre el consumo, es decir financiado por el consumidor final. Un impuesto indirecto es el impuesto que no es percibido por el fisco directamente del tributario. El IVA es percibido por el vendedor en el momento de toda transacción comercial (transferencia de bienes o
-
IVA Acreditable
LAETpiggEl impuesto acreditable es el IVA que los contribuyentes pagan a sus proveedores de bienes o servicios y que pueden disminuir o restar del IVA que a su vez ellos hayan cobrado o hayan trasladado a sus clientes. Esta Cuenta registra los aumentos y disminuciones del impuesto al valor agregado
-
IVA En General
nicolasand1422. Lea cuidadosamente las siguientes oraciones y Subraye la forma correcta del verbo. 7 points 1. Could I speak to Linda? I’m afraid she puts/’s putting the baby to bed. Could you ring back in about half an hour? 2. I first met my husband when I worked/was working in
-
IVA EN VENEZUELA
jpadronLey del Impuesto al Valor Agregado (IVA) de Venezuela La Ley del Impuesto al Valor Agregado en su Artículo 1º nos señala: "es un tributo que grava la enajenación de bienes muebles, la prestación de servicios y la importación de bienes, aplicable en todo el territorio nacional, que deberán pagar
-
Iva Lo Que Dice El Articulo 182 Del Cot
RaizaularEl artículo 82 del COT expresa que: “habrá reincidencia cuando ocurra el imputado después de una sentencia o resolución firme sancionadora, cometiere uno o varios ilícitos tributarios de la misma índoles durante los 5 años contados a partir de aquellos. La reincidencia: no es un delito en sí, es una
-
Ivalides
qwertyuip123IVALIDES Una de las preocupaciones en nuestro país, contenidas en la Carta Magna de 1917 y su Artículo 123, sin duda es la protección social ante la contingencia derivada de enfermedades y accidentes no profesionales en los trabajadores de México. En la XXIX surge hacia el año 1943 la Ley
-
![Iván Dragó participa en el concurso de invención de juegos auspiciado por La Compañía de los Juegos Profundos]()
Iván Dragó participa en el concurso de invención de juegos auspiciado por La Compañía de los Juegos Profundos
SUSA15SIPNOSIS Iván Dragó participa en el concurso de invención de juegos auspiciado por La Compañía de los Juegos Profundos, del que resulta ganador. El único detalle fuera de lo común es que no se anuncia cuál es el premio. Lo que sí sabe es que a partir de ese momento
-
Ivan Pavlov
MiliizIván Pávlov Iván Petróvich Pávlov (en ruso: Ива́н Петро́вич Па́влов), (Riazán, 14 de septiembre de 1849 - San Petersburgo, 27 de febrero de 1936) fue un fisiólogo ruso. Fue hijo de un patriarca ortodoxo.1 Comenzó a estudiar teología, pero la dejó para empezar medicina y química en la Universidad de
-
![Iván Pávlov. ). Psicología y Mente]()
Iván Pávlov. ). Psicología y Mente
Lizbeth ZamoraIván Pávlov Yoselin Zamora Rodríguez Universidad Autónoma De Tlaxcala Su nombre completo es Iván Petrovich Pávlov quien fue reconocido por sus experimentos que realizo con perros los cuales lo llevaron a ganar el premio Novel 1904 de Fisiología , los cuales dieron como resultado al condicionamiento clásico o también conocido
-
Iván Petróvich Pávlov un fisiólogo ruso
alma55Iván Petróvich Pávlov (en ruso: Ива́н Петро́вич Па́влов), (Riazán, 14 de septiembre de 1849 - San Petersburgo, 27 de febrero de 1936), fue un fisiólogo ruso. Fue hijo de un patriarca ortodoxo.1 Comenzó a estudiar teología, pero la dejó para empezar medicina y química en la Universidad de San Petersburgo,
-
Ivanpah
Fernando NuñezCurrículum Vitae I- DATOS PERSONALES: Nombre: Lugar y fecha de nacimiento: Edad: Sexo: Edo. Civil: Nacionalidad: CURP: RFC: Seguro social: Dirección actual: Tel. móvil: Tel. convencional: Correo electrónico: Redes sociales: Tipo sanguíneo: Pasaporte: Visa: IFE: Cartilla militar: (si no se cuenta con algún documento que lleve folio, se le escribe
-
![IVE (Interrupción Voluntaria del Embarazo)]()
IVE (Interrupción Voluntaria del Embarazo)
yatzirirjEl aborto no es una cuestión meramente de creencia sino que se trata de un derramamiento de sangre; no es simplemente sobre puntos de vista sobre víctimas. Padre Frank Pavone CAPITULO I: MARCO CONCEPTUAL 1.1Concepto Médico IVE (Interrupción Voluntaria del Embarazo). Interrupción del embarazo antes de la visibilidad fetal con
-
Ivestigacio De Operaciones
josueurielINSTITUTO TECNOLÓGICO SUPERIOR DE HUICHAPAN INVESTIGACION DE OPERACIONES ALUMNO: JOSUE URIEL RESENDIZ GONZALEZ CATEDRÁTICO: Ing. MARIA ISABEL CARRERA: INGENIERÍA EN SISTEMAS COMPUTACIONALES TRABAJOS Unidad 1: Programación No Lineal 1.1 Definición, desarrollo y tipos de modelos de investigación de operaciones. Es un procedimiento o algoritmo matemático mediante el cual se resuelve
-
Ivestigació Operativa
feradoferadezTRABAJO ACADÉMICO Estimado(a) alumno(a): Reciba usted, la más sincera y cordial bienvenida a la Escuela de DERECHO Y CIENCIA POLITICA de Nuestra Universidad Alas Peruanas y del docente – tutor a cargo del curso. En el trabajo académico deberá desarrollar las preguntas propuestas por el tutor, a fin de lograr
-
Ivestigación
inexpugnabilisCualidades intelectuales del investigador Cualidades del investigador: Todo científico debe contar con algunos elementos básicos para garantizar que su investigación está ajena de prejuicios que comprometan su veracidad: Capacidad de asombro. Aceptar cuestionamientos. Dominio de la materia. Espíritu crítico. Laboriosidad. Trabajo de equipo. Perseverancia. Rectitud del pensamiento y principios éticos.
-
Ivestigacion
javogomezTAREA No. 5 Buscar en fuentes confiables las siguientes definiciones y realizar una ficha de trabajo por cada una. 1. Ciencia http:/es.thefreedictionary.com/ciencia Conjunto organizado de conocimientos sobre una materia determinada, a los que se llega mediante la observación y análisis de sus fenómenos, causas y efectos 2. Teoría, http:/es.thefreedictionary.com/teor%C3%ADa 1
-
![Ivestigación acerca de las bolsas de aire]()
Ivestigación acerca de las bolsas de aire
Cecilia GrijalvaTema de investigación: Bolsas de aire Universidad Politécnica de chihuahua Miembros de equipo: Javier Adrián Hernández Alan Ramón Aguilar Solís Irving Mauricio Valerio Yáñez Fecha de entrega 7 de diciembre 2015 Índice: Introducción.3 Antecedentes.3 Planteamiento del problema.4 Justificación.4 Objetivos…5 Marco teórico.5 Sumario y conclusión.20 Referencias.21 Apendices…22 Introducción Actualmente las empresas